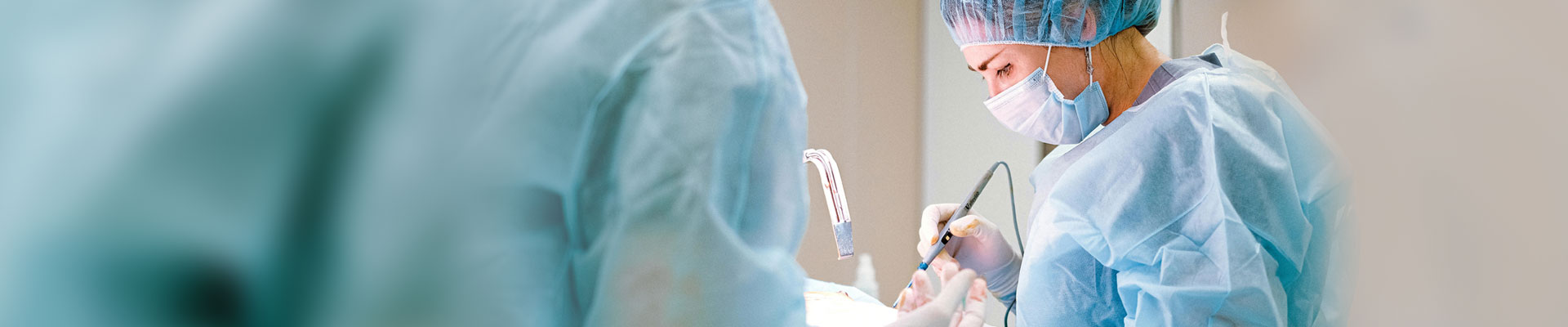

Análise de pontos de controle de qualidade para P&D de polímero de uso únicoclipes de fechamento de tecido para cirurgia laparoscópica
I. Sistema de controle de matéria-prima
De acordo com o princípio básico de "segurança e eficácia" dos dispositivos médicos, o controle de matérias-primas precisa construir um mecanismo de garantia triplo. Em primeiro lugar, estabeleça um arquivo de biocompatibilidade, de acordo com a série ISO 10993 de padrões para citotoxicidade básica de polímeros, alergenicidade e outras avaliações sistemáticas, focando na estabilidade do material' s desempenho antes e depois da esterilização. Em segundo lugar, a gestão dinâmica dos fornecedores é implementada para garantir a consistência dos lotes de matérias-primas por meio de auditorias de voo, e a análise espectral e outras tecnologias são usadas para estabelecer um banco de dados de 'impressões digitais' de materiais. Finalmente, um sistema de rastreabilidade é estabelecido para formar um espectro completo de materiais, desde a aquisição de matérias-primas de grau médico até a modificação e processamento, que atende aos requisitos do sistema de qualidade.

II, desenvolvimento do processo de moldagem
A validação do processo segue a lógica progressiva de 'bloqueio de projeto - otimização de parâmetros - melhoria contínua'. Na fase de desenvolvimento do molde, a tecnologia de análise de fluxo de molde digital é usada para otimizar o projeto do sistema de vazamento para garantir que a cristalinidade dos produtos atenda aos requisitos de propriedades mecânicas. Em termos de controle de processo, é estabelecida uma janela de processo contendo parâmetros-chave, como temperatura, pressão e tempo, e um intervalo de produção robusto é determinado por meio de métodos estatísticos. É dada especial atenção ao impacto dos fatores ambientais na estabilidade dimensional, de acordo com as normas para estabelecer um programa de controle ambiental de sala limpa, monitoramento em tempo real de temperatura e umidade, concentração de partículas.
III. Estudo de adaptabilidade da esterilização
De acordo com as características dos diferentes métodos de esterilização, desenvolver estratégias de verificação. A esterilização por óxido de etileno concentra-se no estudo da adsorção do material no efeito da esterilização, com referência ao estabelecimento padrão do modo de carga máxima/mínima. A esterilização por radiação precisa avaliar o grau de destruição da estrutura da cadeia polimérica por radiação e prever a estabilidade a longo prazo pelo teste de envelhecimento acelerado. Independentemente do modo, é necessário realizar a análise de resíduos e estabelecer um processo de resolução para garantir a conformidade com os requisitos de limite de segurança dos Princípios Orientadores para Avaliação Biológica de Dispositivos Médicos.
IV. Sistema de verificação funcional

Construir um sistema de verificação a três níveis de «ensaio de simulação - ensaio in vitro - ensaio em animais». A verificação básica de desempenho inclui testes de índice mecânico, como retenção da força de fixação e resistência antiderrapante, e o equipamento de teste em conformidade com os padrões ASTM é usado para garantir a confiabilidade dos dados. A validação avançada envolve a construção de um modelo de tecido ex vivo para simular o cenário de pinçamento vascular em cirurgia real. Por fim, a degradação in vivo é observada por meio de experimentos em animais para avaliar o nível de resposta tecidual, e as operações relevantes seguem rigorosamente os requisitos do 'Código para Gestão da Qualidade de Ensaios Clínicos de Dispositivos Médicos'.
V. Mecanismo de Gestão de Riscos
O gerenciamento de riscos é realizado durante todo o ciclo de vida do produto. Na fase de projeto, as ferramentas FMEA são usadas para identificar sistematicamente possíveis modos de falha e estratégias de controle são formuladas para pontos de alto risco, como a confiabilidade da estrutura de travamento e a visibilidade do sistema em desenvolvimento. O processo de produção estabelece um sistema de controle estatístico de processo (SPC) e implementa o monitoramento do valor CPK para os principais processos. O feedback clínico é coletado por meio do sistema de rastreabilidade UDI após a comercialização, formando um ciclo fechado de controle de risco. Todas as atividades estão em conformidade com os requisitos do processo de gerenciamento de riscos da norma ISO 14971.
VI. Controle de Transformação da Produção
Ao fazer a transição do laboratório para a industrialização, o foco está em resolver o problema de equivalência do aumento de escala do processo. Através do planejamento de experimentos (DOE) para verificar o efeito scale-up do equipamento, e estabelecer o modelo de conversão de parâmetros do processo. Implemente o design para fabricação (DFM) para otimizar a estrutura do produto e adote conceitos de design modular para melhorar a eficiência da montagem automatizada. O link de Triagem de Estresse Ambiental (ESS) simula cenários reais, como transporte e armazenamento, para garantir que a robustez do produto atenda aos requisitos da norma YY/T 0681.15 para sistema de barreira estéril.

VI, construção do sistema de qualidade
Tomando como estrutura o sistema de gestão da qualidade ISO 13485, estabeleça um sistema de controle de documentos que cubra todo o processo de pesquisa e desenvolvimento. Incluindo documentos de projeto e desenvolvimento, relatórios de verificação de processo, registros de teste e outros sistemas de documentos de três níveis. Em particular, o gerenciamento de controle de mudanças é fortalecido e a avaliação de impacto e a reverificação são necessárias para quaisquer mudanças em materiais, processos ou equipamentos. Auditorias internas regulares e análises de gestão são realizadas para garantir a conformidade contínua com os requisitos das 'Boas Práticas de Fabricação para Dispositivos Médicos'
+86 18361958211
marketing@cndonho.com
+86 18361958211
No.2 Zhiwei Road, Qiandeng Town, Kunshan City, Jiangsu Province, China




